![absoluteantibody/Anti-DNA/RNA G-quadruplex (and related small molecules) [BG4]/100 μg/Ab00174-24.1](images/no_picture.gif)
UniProtAccessionNumberofTargetProtein:n/a
Immunogen:DNA/RNAG-quadruplex.
Specificity:BindswithhighselectivityandlownanomolaraffinitytoDNAandRNAG-quadruplexstructures.
ApplicationNotes:Thisantibodyhasbeenshown(byELISA)tobindselectivelytoG-quadruplexformingDNAandRNAstructures.PleasenotethatunliketheoriginalscFvreportedbyBiffietal.,thisantibodydoesnothaveFLAG-tag.Weldonetal.(2016,PMID:27820800)usedAb00174-1.1toidentifyG-quadruplexesinlongfunctionalRNAsusinganelectrophoreticmobilityshiftassay(EMSA).BG4wasshowntohaveweakcross-reactivitywithiMotifstructures(2018,PMID:29686376).iMotifstructurescanselectivelybedetectedusingouranti-iMotifantibodyAb01462.
Antibodyfirstpublishedin:BiffiG, TannahillD, McCaffertyJ, BalasubramanianS.QuantitativevisualizationofDNAG-quadruplexstructuresinhumancells.NatChem. 2013Mar;5(3):182-6.PMID:23422559Noteonpublication:DescribesgenerationofaG-quadruplex-specificantibodyusingphagedisplayandtheinvitroselection(usingELISAandCD)ofastructure-specificantibodyprobethatbindswithhighselectivityandlownanomolaraffinitytoDNAG-quadruplexstructurescalledBG4.
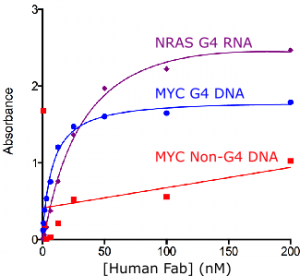
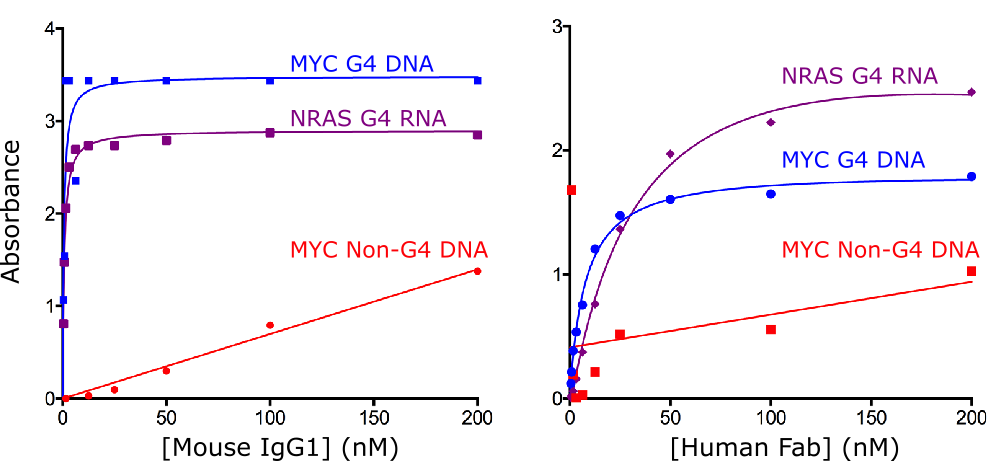
ComparisonofthebindingoffulllengthIgGandFabversionsoftheBG4antibodyBindingcurvesfortheassociationofBG4asafull-lengthmurineIgG1(leftpanel)andahumanFabfragment(rightpanel)withaDNAG-quadruplexoligo(fromhumanMYCgenepromoter:5’[Btn]TGAGGGTGGGTAGGGTGGGTAA),aRNAG-quadruplexoligo(frumhumanNRAS5’UTRRNA:5’[Btn]TGAGGGTGGGTAGGGTGGGTAA)andanon-G-quadruplexformingnegativecontrololiogo(mutatedMYCsequence:5′[Btn]TGAGAGTGAGTAGAGTGAGTAA)asdeterminedbyELISA.ToformtheG-quadruplex,theoligos(at5uM)wereannealedin10mMTris,100mMKCl(pH7.4)andheatedto95°Cfor10minutesbeforeslowlycoolingtoRT.TheELISAwasperformedbybindingthebiotinylatedoligos(50nM)toasteptavidinplatefor1hour.Afterwashing,theplatewasblockedandincubatedwithserialdilutionsofantibodyfor1houratRT.Theplateswerewashedandthenincubatedwithananti-mouseoranti-human,HRP-coupledsecondaryantibody.Afterwashing,TMBsubstratewasadded,thereactionstoppedwithHClandtheabsorbancemeasuredat450nmonaplatereader.Eachexperimentaldatapointwasdeterminedintriplicate.ThismethodisdescribedintheNatureChemistrypaper(doi:10.1038/NCHEM.1548,dos:10.1038/NCHEM.1805).DatacourtesyofDarcieMulhearnandDr.DavidTannahill,BalasubramanianGroup,DepartmentofChemistry,UniversityofCambridge.
ebiomall.com






>
>
>
>
>
>
>
>
>
>
>
>
常用流动相加酸碱后PH的总结,希望大家能够提供一点自己测过的结果,谢谢先
1.直接用固体磷酸钠配制成50mM的磷酸钠溶液,再调pH到7.4;(我们试着用这个做了下,发现挂不上柱)
2.配置磷酸钠盐缓冲液:按NaH2PO4:Na2HPO4以19:81的摩尔比配制成pH7.4的缓冲液?(附一张百度出来的配方
)
3.如果是磷酸钠盐缓冲液,可以直接将50mM的NaH2PO4的水溶液用NaOH调成pH7.4吗?
再者,2和3这两个方法配制的磷酸钠盐缓冲液有什么区别?最终效果是一样的吗?如果不一样,有什么理论的知识支撑呢?个人感觉是分析化学中酸碱理论中的缓冲液那里的知识。求帮忙解答这些疑问。
另外,我还想问一下,pH对于Ni柱对His-tagged的蛋白的分离纯化影响大吗?是怎么影响的?谢谢大家了!
有了源数据之后把源数据按照大小排列,
选中源数据区域-->ALT+A1-->选中图标区右键-->更改图表类型-->散点图
因为是考察不同PH对药物的影响,样品又不好改变其PH值,这种情况怎么办?希望有经验的高手指教。
我的流动相是甲醇-水(90:10)
谢谢赐教!
请进子版按格式发贴,自行修改,谢谢。
由弱酸及其盐、弱碱及其盐组成的混合溶液,能在一定程度上抵消、减轻外加强酸或强碱对溶液酸碱度的影响,从而保持溶液的pH值相对稳定。这种溶液称为缓冲溶液。
:)
我在做一细菌不同酸碱度生长状况时,发现这些奇怪现象:pH=3的培养基灭菌(TSB液体培养基)灭菌后pH上升到到9.2!而原来pH=9.0的降到8.7(基本没多少变化),请问各位大侠,这是什么原因?
一般做不同酸碱度生长实验时,该如何才能防止pH在湿热灭菌后基本不变化?
是否可以理解为纯化水得PH范围为6.3-7.6?能否直接用pH计测量?谢谢!









