

公司背景:SICGEN抗体是一家葡萄牙生物技术公司,专门研发和生产用于生命科学研究的抗体。公司利用尖端技术,以最优的质量和最具竞争力的价格,致力于成为世界多克隆抗体及抗体相关产品和服务的提供商。它既是一个产品公司也是一个服务公司,它的主要业务是发现和销售用于研究和科学目的的新抗体。多年来,SICGEN一直为国内外主要大学、科研机构、制药企业和生物技术公司生产定制的多克隆抗体。
Biotechrabbit为诊断、生命科学研究与应用市场创新、开发和生产性能卓越的分子生物学产品。所有的开 发、生产与物流均在我们的柏林工厂进行。分子生物酶及蛋白的生产是Biotechrabbit的支柱业务。我们采用高密度原核与真核发酵,之后以数道经过精确调整的纯化步骤生产高纯度蛋白,可进行小样和大规模生产。研发部门由经验丰富的科学家及业务开发人员组成,重点关注客户及合作伙伴的需求。我们的团队专心致力于提供用于分子生物学领域的顶级品质产品。

对单一和多重靶标均具有同类最佳性能
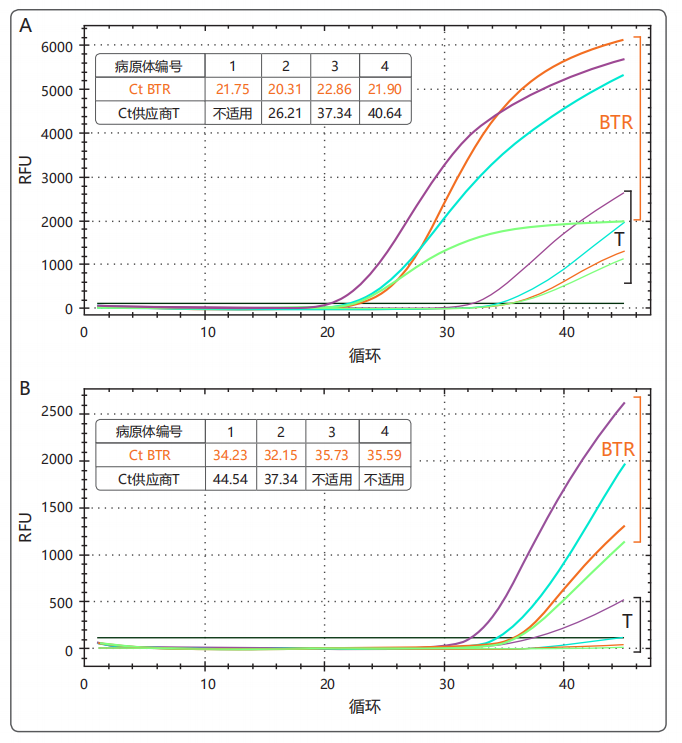
在病原体检测方面具有高度特异性的便捷预混液
对低丰度DNA靶标高度灵敏
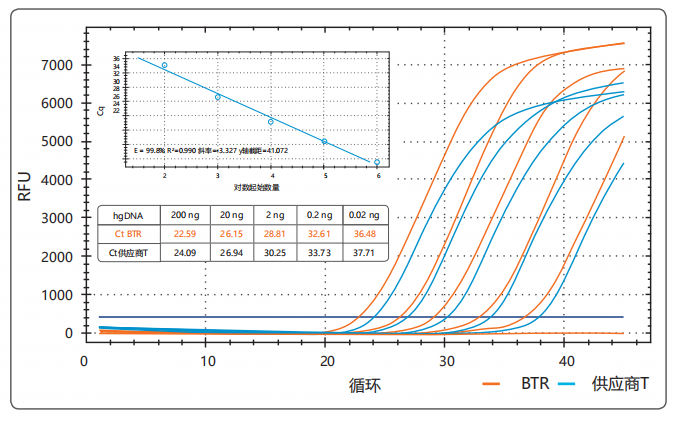
BiotechrabbitCAPITALqPCR ProbeMix预混液用于对基因组、CDNA和病毒序列进行定量分析,在单一和多重qPCR方面都具备卓越的性能。该预混液的高灵敏性非常适合于诸如病原体检测等应用中检测低丰度DNA靶标。
ebiomall.com






>
>
>
>
>
>
>
>
>
>
>
首先,给大家先分享一下有关细胞的基本知识。
细胞培养过程中绝对避免如细菌,支原体,真菌的污染,这些污染将显著地影响并改变实验结果。细胞培养因组织来源的不同而异,动物细胞一般采用黏附培养或者悬浮培养。根据其增殖潜力不同而被分为三类:原代细胞,细胞株,细胞系。
贴壁细胞:黏附细胞需要附着后才能生长,不断增殖的细胞在细胞培养器皿上铺成单细胞层。许多细胞在铺满细胞培养器壁后就不再增殖,有些细胞在此之后会死亡。从组织中得到的大多数细胞都是贴壁细胞。
悬浮细胞:悬浮细胞在培养基中存活和增殖,不需要黏附在细胞培养器皿上,包括造血干细胞(来源于血液,骨髓,脾脏),一些转化的细胞系以及恶性肿瘤细胞等。
原代细胞:由酶法、化学法或者机械法得到的组织碎片中的细胞迁移到细胞培养皿上形成了原代细胞,这些细胞在分散组织的过程中幸存下来,黏附或者悬浮于细胞培养液中,之后进行增殖。这些细胞不能或者仅能进行有限的细胞分裂,分裂相结束后进行衰老相,最后死亡。黏附原代培养细胞对接触抑制特别敏感,一旦铺满细胞培养皿他们就停止生长。培养原代细胞通常比培养细胞系更加困难。在实验中有时需要用到原代细胞而不是细胞系。
细胞株:从原代细胞开始的头几次传代所得到的细胞被称为细胞株。这些细胞传代几次后就衰老了,但可以导入病毒的转化因子增加细胞株的增殖代数。这些细胞的表型介于细胞株和细胞系之间,他们可以更长时间的增殖,但最终他们和细胞株一样也会衰老,停止分裂。在筛选稳定转化的细胞克隆时,使用这些细胞比原代细胞更方便。
细胞系:细胞株最终都会死亡,但他们中的某些个体发生了一些可稳定遗传的突变,这些突变使得这些细胞能够无限的增殖。这类细胞和它的后代被称为细胞系,这个过程被称为体外转化或永生化,这和体内的细胞癌变相似。无论是自发还是经过某种诱变剂的诱导,龋齿类动物的原代细胞会更容易形成细胞系。相比较而言,人的原代细胞很少会形成细胞系,但是从人癌组织中分离得到的细胞通常是永生的,可以传代成细胞系。细胞系比原代细胞和细胞株更易于使用。
下面简单先提几个问题:
问题:细胞污染问题解决(操作注意事项和污染源分析)
小编回复:
安全操作须知:操作所有可能具有感染性的材料应当遵循以下原则:操作细胞时严格按照细胞操作规程以最大可能避免操作者和细胞中可能带有的致病因子接触,操作细胞应当在合格的层流超净台中进行,注意无菌并且避免气溶胶的生成。操作完成后,所产生的废弃物应当用湿热灭菌或浸没在合适的去感染物溶液中。
无菌操作和尽量避免气溶胶产生所用的器械和溶液应该事先经过彻底灭菌,工作之前用消毒液擦拭台面,试剂瓶和手。操作过程避免形成气溶胶,吸入气溶胶是有害的。气溶胶也有可能会导致细胞之间的交叉污染。因此,应选用TD(todeliver)吸管而不是TC(tocontain)吸管,所用的吸管后端应该塞上棉花。混合溶液时避免快速的吸上吸下,吹出的液体时不要用力过猛。移液时移液管口尽量与培养瓶中液面接近。使用离心机时确保离心管盖是合上的,避免液滴残留在离心管盖附近。使用带盖的离心转头时,运行前务必盖紧。
使用层流超净台:保证层流超净台放置地方的气流不被经常搅动。避免把它安置在门口,通气口或经常有人活动的地方。超净台应放在专门的细胞培养间内。保持超净台的整洁,不把东西堆放在里面。工作之前,给工作台面和试剂瓶外表面消毒,把所有细胞操作作用到的东西都放在超净台内。有序排列器械,吸管,试剂瓶和垃圾杯,把用过的物品和干净的物品分开摆放。移动废物品时避免从干净的物品上经过。
细胞污染:细胞污染物会抑制细胞的生长,导致细胞死亡,使实验结果不一致。无论是细胞培养新手还是老手都会出现这样的问题。可以导致污染的途径举不胜举,例如不规范的操作,被污染的培养基,试剂,器械(如枪头),或是携带在操作者身上和来自其他实验室中的微生物。在动物细胞培养中,细菌,真菌,霉菌,支原体和其他种类细胞是常见的污染物。规范的操作可以帮助避免细胞被微生物和其他种类的细胞污染。为了减少偶尔细胞污染所造成的损失,我们建议冻存细胞保种,即使细胞被污染了也能够及时补充新的细胞。
微生物污染:细胞微生物污染后,有些情况下细胞培养基会变浑浊,pH值发生显著变化(通常为细菌污染)。另一些情况下,微生物污染不会使细胞培养液变浑浊,对细胞也不会产生明显的影响。例如支原体污染是一种极为常见,但极难检测到的微生物污染。
支原体污染-检测:支原体是一些体型小,生长缓慢的原核生物,它们没有细胞壁,是常见的细胞污染微生物。常用的抗生素和抗真菌药一般对支原体都没有作用。更糟糕的是,由于支原体一般不会比细胞生长更快也就不会引起细胞培养基的浑浊度和颜色变化,所以它们会长时间存在而不被发现,并会迅速传播到其他细胞中去。支原体污染会抑制细胞的代谢和生长,也会干扰细胞的核酸代谢和细胞的抗原性。急性的支原体感染会使所有的细胞状态变坏,有时候有个别细胞会形成克隆。有三种主要的检测支原体的方法:Hoeschest33258染色;支原体特异的DNA探针(FisherScientifie);基于PCR的方法(如MinervaBiolabs的VenorGeMMycoplasmaDetectionKit)。另外,ATCC和MicroBIOLOGicalAssociates都提供付费的基于PCR的支原体检测服务。
支原体污染-清除:处理支原体慢性污染的细胞最明智的方法是丢弃它,用湿热灭菌或焚烧彻底消灭污染物。处理的方法主要是用各种商业化的抗生素处理,如Mynox®MycoplasmaEliminationReagent(MinervaBiolabs),enrofloxacin(Baytril®),及tiamulin和minocycline的混合处理(BM-Cyclin)。
细胞的交叉污染:细胞被另一种快速生长的细胞污染是较为严重的问题。为避免交叉污染,需要向可以保证质量的细胞库订购细胞,在超净台中一次只处理一种细胞,给不同的细胞分别准备所需的枪头,试剂,培养基。并且定期检查细胞的形态和生长特征。
启动子是RNA聚合酶能够识别并与之结合,从而起始基因转录的一段DNA序列,通常位于基因上游.一个典型的启 动子包括CAAT-box和TATA-box,它们分别依赖DNA的RNA聚合酶的识别和结合位点,一般位于转录起始位点上游几十个碱基处.在核心启动子上 游通常会有一些特殊的DNA序列,即顺式作用元件,转录因子与之结合从而激活或抑制基因的转录.一旦RNA聚合酶定位并结合在启动子上即可 启动基因转录,因此启动子是基因表达调控的重要元件,它与RNA聚合酶及其他蛋白辅助因子等反式作用因子的相互作用是启动子调控基因转录的实质.
根据启动子的转录模式可将其分为3类:组成型启动子、组织或器官特异性启动子和诱导型启动子.
目标基因全长1800bp,通过重叠延伸的方式获得的自杀敲除组件,左右同源序列均为500bp左右,构建自杀载体(确认载体没有问题),期望进行目标基因的失活处理,但将近1个月的时间,不见任何目的克隆,故在此请各位战友指点。
采用电转的方式将自杀载体(约6700bp)导入黄色短杆菌,感受态的细胞制备采用相关文献方式,甘氨酸和吐温-30的方式进行摇菌并制备电转感受态,1800v电转(电压进行过梯度,1200、1500、1800、2200、2500。1800v效果相对较好,故选之),但电转效率仍是较低,复苏2h,浓缩涂板LBG+kan(kan浓度20ug/ml),平板克隆很少,几次都只有20个左右的克隆。
1)克隆很少,原因可能跟菌株的电转效率有关,不知战友有没有谷氨酸棒杆菌或黄色短杆菌相关较好的电转经验,还请指教?
2)抗性平板克隆很少,还可能和重组效率有关,但根据pk18mobsacB质粒的特性,既然能在抗性平板生长,理论上应该是已经进行了一次重组了,但结果是不管我用pk18载体本身的Kan序列引物还是最终诱导进行PCR验证,均未证实到一次重组的发生,更不要说获得敲除失活的目的菌株了。问题是这个带有抗性的克隆到底是携带了什么使其同样具有抗性(显微检验不是杂菌)?如何有效提高或促进自杀载体在宿主内的重组效率呢?或是更有效的准确的检测验证手段??
3)利用自杀载体的方式进行黄色短杆菌(或谷氨酸棒杆菌)的基因敲除缺失比较不易,不知有没有正在做这方面相关研究的战友,希望能够多多交流和学习。。。
不知道我的疑惑讲清楚了没有,若哪里不清楚还请指出,我再细说。。。期望xdjm们的帮助啊。。。先谢过了。。
在生物体内发现主要有三种不同的RNA分子在基因的表达过程中起重要的作用。它们是信使RNA(messengerRNA,mRNA)、转运RNA(tranfer RNA,tRNA)、核糖体RNA(ribosomal RNA,rRNA)。RNA含有四种基本碱基,即腺嘌呤、鸟嘌呤、胞嘧啶和尿嘧啶。此外还有几十种稀有碱基。
RNA的一级结构主要是由AMP、GMP、CMP和UMP四种核糖核苷酸通过3',5'磷酸二酯键相连而成的多聚核苷酸链。天然RNA的二级结构,一般并不像DNA那样都是双螺旋结构,只有在许多区段可发生自身回折,使部分A-U、G-C碱基配对,从而形成短的不规则的螺旋区。不配对的碱基区膨出形成环,被排斥在双螺旋之外。RNA中双螺旋结构的稳定因素,也主要是碱基的堆砌力,其次才是氢键。每一段双螺旋区至少需要4~6对碱基对才能保持稳定。在不同的RNA中,双螺旋区所占比例不同。【RNA的二级结构】细胞内有三类主要的核糖核酸,即:mRNA、rRNA、tRNA。它们各有特点。在大多数细胞中RNA的含量比DNA多5~8倍。【大肠杆菌RNA的性质】
mRNA
生物的遗传信息主要贮存于DNA的碱基序列中,但DNA并不直接决定蛋白质的合成。而在真核细胞中,DNA主要贮存于细胞核中的染色体上,而蛋白质的合成场所存在于细胞质中的核糖体上,因此需要有一种中介物质,才能把DNA 上控制蛋白质合成的遗传信息传递给核糖体。现已证明,这种中介物质是一种特殊的RNA。这种RNA起着传递遗传信息的作用,因而称为信使RNA(messenger RNA,mRNA)。
mRNA的功能就是把DNA上的遗传信息精确无误地转录下来,然后再由mRNA的碱基顺序决定蛋白质的氨基酸顺序,完成基因表达过程中的遗传信息传递过程。在真核生物中,转录形成的前体RNA中含有大量非编码序列,大约只有25%序列经加工成为mRNA,最后翻译为蛋白质。因为这种未经加工的前体mRNA(pre-mRNA)在分子大小上差别很大,所以通常称为不均一核RNA(heterogeneous nuclear RNA,hnRNA)。
tRNA
如果说mRNA是合成蛋白质的蓝图,则核糖体是合成蛋白质的工厂。但是,合成蛋白质的原材料——20种氨基酸与mRNA的碱基之间缺乏特殊的亲和力。因此,必须用一种特殊的RNA——转运RNA(transfer RNA,tRNA)把氨基酸搬运到核糖体上,tRNA能根据mRNA的遗传密码依次准确地将它携带的氨基酸连结起来形成多肽链。每种氨基酸可与1-4种tRNA相结合,现在已知的tRNA的种类在40 种以上。
tRNA是分子最小的RNA,其分子量平均约为27000(25000-30000),由70到90个核苷酸组成。而且具有稀有碱基的特点,稀有碱基除假尿嘧啶核苷与次黄嘌呤核苷外,主要是甲基化了的嘌呤和嘧啶。这类稀有碱基一般是在转录后,经过特殊的修饰而成的。
1969年以来,研究了来自各种不同生物,:如酵母、大肠杆菌、小麦、鼠等十几种tRNA的结构,证明它们的碱基序列都能折叠成三叶草形二级结构(图3-23),而且都具有如下的共性:
① 5’末端具有G(大部分)或C。
② 3’末端都以ACC的顺序终结。
③ 有一个富有鸟嘌呤的环。
④ 有一个反密码子环,在这一环的顶端有三个暴露的碱基,称为反密码子(anticodon).反密码子可以与mRNA链上互补的密码子配对。
⑤ 有一个胸腺嘧啶环。
rRNA
核糖体RNA(ribosomal RNA,rRNA)是组成核糖体的主要成分。核糖体是合成蛋白质的工厂。在大肠杆菌中,rRNA量占细胞总RNA量的75%-85%,而tRNA占15%,mRNA仅占3-5%。
rRNA一般与核糖体蛋白质结合在一起,形成核糖体(ribosome),如果把rRNA从核糖体上除掉,核糖体的结构就会发生塌陷。原核生物的核糖体所含的rRNA有5S、16S及23S三种。S为沉降系数(sedimentation coefficient),当用超速离心测定一个粒子的沉淀速度时,此速度与粒子的大小直径成比例。5S含有120个核苷酸,16S含有1540个核苷酸,而23S含有2900个核苷酸。而真核生物有4种rRNA,它们分子大小分别是5S、5.8S、18S和28S,分别具有大约120、160、1900和4700个核苷酸。
rRNA是单链,它包含不等量的A与U、G与C,但是有广泛的双链区域。在双链区,碱基因氢键相连,表现为发夹式螺旋。
rRNA在蛋白质合成中的功能尚未完全明了。但16 S的rRNA3’端有一段核苷酸序列与mRNA的前导序列是互补的,这可能有助于mRNA与核糖体的结合。
snRNA
除了上述三种主要的RNA外,细胞内还有小核RNA(small nuclearRNA,snRNA)。它是真核生物转录后加工过程中RNA剪接体(spilceosome)的主要成分。现在发现有五种snRNA,其长度在哺乳动物中约为100-215个核苷酸。snRNA一直存在于细胞核中,与40种左右的核内蛋白质共同组成RNA剪接体,在RNA转录后加工中起重要作用。另外,还有端体酶RNA(telomeraseRNA),它与染色体末端的复制有关;以及反义RNA(antisenseRNA),它参与基因表达的调控。
有的RNA分子还具有生物催化作用。
上述各种RNA分子均为转录的产物,mRNA最后翻译为蛋白质,而rRNA、tRNA及snRNA等并不携带翻译为蛋白质的信息,其终产物就是RNA。
2006诺贝尔医学奖成果RNA干扰机制解读
1990年,曾有科学家给矮牵牛花插入一种催生红色素的基因,希望能够让花朵更鲜艳。但意想不到的事发生了:矮牵牛花完全褪色,花瓣变成了白色!科学界对此感到极度困惑。
类似的谜团,直到美国科学家安德鲁·法尔和克雷格·梅洛发现RNA(核糖核酸)干扰机制才得到科学的解释。两位科学家也正是因为1998年做出的这一发现而荣获今年的诺贝尔生理学或医学奖。
根据法尔和梅洛的发现,科学家在矮牵牛花实验中所观察到的奇怪现象,其实是因为生物体内某种特定基因“沉默”了。导致基因“沉默”的机制就是RNA干扰机制。
此前,RNA分子只是被当作从DNA(脱氧核糖核酸)到蛋白质的“中间人”、将遗传信息从“蓝图”传到“工人”手中的“信使”。但法尔和梅洛的研究让人们认识到,RNA作用不可小视,它可以使特定基因开启、关闭、更活跃或更不活跃,从而影响生物的体型和发育等。
诺贝尔奖评审委员会在评价法尔和梅洛的研究成果时说:“他们的发现能解释许多令人困惑、相互矛盾的实验观察结果,并揭示了控制遗传信息流动的自然机制。这开启了一个新的研究领域。”
科学家认为,RNA干扰技术不仅是研究基因功能的一种强大工具,不久的未来,这种技术也许能用来直接从源头上让致病基因“沉默”,以治疗癌症甚至艾滋病,在农业上也将大有可为。从这个角度来说,“沉默”真的是金。美国哈佛医学院研究人员已用动物实验表明,利用RNA干扰技术可治愈实验鼠的肝炎。
目前,尽管尚有一些难题阻碍着RNA干扰技术的发展,但科学界普遍对这一新兴的生物工程技术寄予厚望。这也是诺贝尔奖评审委员会为什么不坚持研究成果要经过数十年实践验证的“惯例”,而破格为法尔和梅洛颁奖的原因之一。
诺贝尔生理学或医学奖评审委员会主席戈兰·汉松说:“我们为一种基本机制的发现颁奖。这种机制已被全世界的科学家证明是正确的,是给它发个诺贝尔奖的时候了。”
补充
核糖核酸(缩写为RNA,即Ribonucleic Acid),存在于生物细胞以及部分病毒、类病毒中的遗传信息载体。
RNA由核糖核苷酸经磷酯键缩合而成长链状分子。一个核糖核苷酸分子由磷酸,核糖和碱基构成。RNA的碱基主要有4种,即A腺嘌呤,G鸟嘌呤,C胞嘧啶,U尿嘧啶。其中,U(尿嘧啶)取代了DNA中的T胸腺嘧啶而成为RNA的特征碱基。
与DNA不同,RNA一般为单链长分子,不形成双螺旋结构,但是很多RNA也需要通过碱基配对原则形成一定的二级结构乃至三级结构来行使生物学功能。RNA的碱基配对规则基本和DNA相同,不过除了A-U、G-C配对外,G-U也可以配对。
在细胞中,根据结构功能的不同,RNA主要分三类,即tRNA(转运RNA), rRNA(核糖体RNA), mRNA(信使RNA)。mRNA是合成蛋白质的模板,内容按照细胞核中的DNA所转录;tRNA是mRNA上碱基序列(即遗传密码子)的识别者和氨基酸的转运者;rRNA是组成核糖体的组分,是蛋白质合成的工作场所。
在病毒方面,很多病毒只以RNA作为其唯一的遗传信息载体(有别于细胞生物普遍用双链DNA作载体)。
1982年以来,研究表明,不少RNA,如I、II型内含子,RNase P,HDV,核糖体大亚基RNA等等有催化生化反应过程的活性,即具有酶的活性,这类RNA被称为核酶(ribozyme)。
20世纪90年代以来,又发现了RNAi(RNA interference,RNA干扰)等等现象,证明RNA在基因表达调控中起到重要作用。
在RNA病毒中,RNA是遗传物质,植物病毒总是含RNA。近些年在植物中陆续发现一些比病毒还小得多的浸染性致病因子,叫做类病毒。类病毒是不含蛋白质的闭环单链RNA分子,此外,真核细胞中还有两类RNA,即不均一核RNA(hnRNA)和小核RNA(snRNA)。hnRNA是mRNA的前体;snRNA参与hnRNA的剪接(一种加工过程)。自1965年酵母丙氨酸tRNA的碱基序列确定以后,RNA序列测定方法不断得到改进。目前除多种tRNA、5SrRNA、5.8SrRNA等较小的RNA外,尚有一些病毒RNA、mRNA及较大RNA的一级结构测定已完成,如噬菌体MS2RNA含3569个核苷酸。
2、基因表达载体的构建
(1)目的:使目的基因在受体细胞中稳定存在并且可以遗传给下一代并表达和发挥作用.(2)基因表达载体的组成:目的基因+启动子+终止子+标记基因
②启动子在基因的首段,它是RNA聚合酶的结合位点,能控制着转录的开始,故②正确;
③终止子在基因的尾端,它控制着转录的结束,故③正确;
④由于受体细胞有植物、动物以及微生物之分,以及目的基因导入受体细胞的方法不同,因此基因表达载体的构建是不完全相同的,
RNAi (RNA interference) 即RNA干涉,是近年来发现的在生物体内普遍存在的一种古老的生物学现象,是由双链RNA(dsRNA)介导的、由特定酶参与的特异性基因沉默现象,它在转录水平、转录后水平和翻译水平上阻断基因的表达。
RNAi的定义
目前对RNAi (RNA interference)的定义有很多种,不同的资料对其定义的侧重点也不尽相同,如果将RNAi看作一种生物学现象,可以有以下定义:① RNAi是由dsRNA介导的由特定酶参与的特异性基因沉默现象,它在转录水平、转录后水平和翻译水平上阻断基因的表达。② RNAi是有dsRNA参与指导的,以外源和内源mRNA为降解目标的转基因沉默现象。具有核苷酸序列特异性的自我防御机制,是一种当外源基因导入或病毒入侵后,细胞中与转基因或入侵病毒RNA同源的基因发生共同基因沉默的现象。
如果将其作为一门生物技术,则定义为:① RNAi 是指通过反义RNA与正链RNA 形成双链RNA 特异性地抑制靶基因的现象,它通过人为地引入与内源靶基因具有相同序列的双链RNA(有义RNA 和反义RNA) ,从而诱导内源靶基因的mRNA 降解,达到阻止基因表达的目的。② RNAi是指体外人工合成的或体内的双链RNA(dsRNA)在细胞内特异性的将与之同源的 mRNA降解成21nt~23nt 的小片段,使相应的基因沉默。③ RNAi是将与靶基因的mRNA 同源互补的双链RNA(dsRNA ) 导入细胞,能特异性地降解该mRNA ,从而产生相应的功能表型缺失, 属于转录后水平的基因沉默(post - transcriptional gene silence , PTGS)。
各种不同定义虽然说法不同,但所描述事实是大体相同的,简单地可以说,RNAi就是指由RNA介导的基因沉默现象。
原理
最近由于RNA干扰(RNA interference,RNAi)的发现使反义领域的研究增多。这种自然发生的现象最早是在秀丽线虫中发现的(1),是序列特异性地使转录后的基因沉默的有力机制。由于最近两年在RNAi领域取得的进步,已经有许多这方面的综述发表(2-4)。RNA干扰是由长的双链RNA分子发动的,该分子可以被Dicer enzyme加工成长度为21-23个核苷酸的RNA(见图)。RNaseIII蛋白被认为是作为一个二聚体发挥作用,它对双链RNA的两个链都进行切割,酶切的产物3'末端互相重叠。然后这种小的干扰RNA分子(small interfering RNAs,siRNAs)掺入RNA诱导的沉默复合物(RNA-induced silencing complex,RISC),引导核酸酶降解靶RNA。
这种保守的生化机制可用于研究多种模式生物的基因功能,但是它在哺乳动物细胞中的应用受到阻碍,因为长的双链RNA分子会引起干扰素应答。因此Tuschi及其同事表明长度为21nt的siRNA可以特异性的抑制哺乳动物细胞基因表达是一个革命性的突破(5)。这个发现激发了大量利用RNAi技术对哺乳动物细胞的研究,因为与传统的反义技术比,RNAi的性能明显较高。
有趣的是,除了短双链RNA,短发夹RNA(short hairpin RNA,shRNA),比如茎环结构在细胞内经过加工后也可以变成siRNA,从而产生RNA干扰(6、7)。这使得构建表达干扰RNA的载体,从而使哺乳动物细胞内基因表达长期沉默成为可能(4、8)。shRNA可以利用RNA聚核酶III启动子转录,在正常情况下,该启动子是控制小核RNA(small nuclear RNA,snRNA)U6(6、7、9、10)或者RNaseP的组分H1 RNA(11)转录的。另外一种办法是两段短RNA分子分别用U6启动子转录出来(6、12、13)。载体介导的siRNA表达使对功能缺失(loss-of-function)表型进行长期分析成为可能。在稳定转染的细胞内,两个月后仍可观察到沉默现象(11)。
另外一种延长siRNA抑制基因表达时间的方法是对化学合成的RNA进行核苷酸修饰。尽管未经修饰的短双链RNA在细胞培养物或者体内的稳定性出乎意料的高,然而有些情况下,需要对siRNA的稳定性进行进一步提高。因此,可以在两条链的末端都引入经过修饰的核苷(14)。一个5'端为两个2'-O-甲基RNA、3'端为4个甲基化核苷的siRNA与序列相同但是未经修饰的siRNA比活性相同,但是在细胞培养物中引起的基因沉默现象的时间延长。然而,增多siRNA中的甲基化核苷,或者在核苷中引入体积较大的烯丙基将导致siRNA活性下降。
RNA干扰在哺乳动物体内的第一个研究是利用快速注射大量生理溶液的方法将一个编码shRNA的质粒注入老鼠的尾静脉(15、16)。在大多数器官中,报道基因(编码于共转染质粒或者转基因小鼠上)的表达可以被有效地抑制。另外,Fas基因被作为肝损伤治疗相关的内源靶标进行了RNA干扰实验(17)。注射siRNA之后,小鼠肝细胞中的Fas mRNA和蛋白水平下降了10天。把Fas基因沉默可以保护小鼠免遭由注射竞争性Fas特异抗体引起的爆发性肝炎,82%用siRNA处理的小鼠活过了10天观察期,而所有的对照小鼠在3天之内死亡。
上述研究中采用的高压导入技术是一种粗暴的方法,不适于治疗用。因此,标准的基因治疗所采用的方法被用于RNA干扰。一个反转录病毒载体被用于导入siRNA,以抑制人类胰腺肿瘤细胞中的癌基因K-ras等位基因(18)。负调控癌细胞中K-ras基因的表达使得它们在注入无胸腺的裸鼠皮下之后不再具有形成肿瘤的能力。这项研究还表明siRNA的高度特异性,因为只有癌基因K-ras被沉默,而与之只有1个碱基对差异的野生型等位基因并没有被沉默。另外,当在纹状区注射表达siRNA的腺病毒之后,转基因小鼠大脑中GFP基因的表达可以被抑制(19)。β-葡萄糖醛酸苷酶(b-glucoronidase)的活性可以通过在小鼠尾静脉注射重组腺病毒抑制。有趣的是,具有CMV启动子和最小的polyA尾的RNA聚合酶II表达元件被用于这个实验,为设计组织特异性或者可诱导的siRNA载体打开了大门。
总的来说,siRNA的第一个体内实验已经进行,其他有重要意义的基因有望于很快作为靶标开展研究。至今为止的研究没有观察到任何应用siRNA引起的毒性作用,但是在治疗人类疾病的临床试验开始之前仍需小心,以排除长期使用RNA干扰引起的严重副作用。因为用siRNA使基因表达沉默与传统的反义技术相似,研究者将从十多年来反义技术研究的教训中获益,比如需要使用合适的对照以证明基因表达的敲除是特异性的,以及对免疫系统可能引起的意外影响进行详细分析。
应用
siRNA可用于研究基因的功能,可是后基因组时代的今天,研究人员已经不满足于一个一个基因沉默这样的研究节奏了,功能基因组学的研究更需要一个能站在全局高度研究多个基因之间关系的工具,因此,用作大规模RNA干扰用的shRNA/siRNA文库应运而生。 shRNA/siRNA文库联合使用高通量筛选技术和高内涵图像分析技术,使得RNAi筛选在反向基因组学、功能基因研究、药物发现等多个领域成为了一个 强大的应用工具。
北京赛诺亚生物技术有限责任公司(http://www.sirnoa.com/)是一家拥有独立自主产权的、以RNAi筛选的相关产品和技术服务为重点生物高新技术企业。公司专业从事各种高通量miRNA检测、RNA干扰筛选、药物筛选、文库筛选及相关产品的研发和销售,同时提供进行各种RNAi相关的载体构建、病毒包装 服务和细胞生物学试剂。公司致力于为从事生命科学研究和早期药物研发的科研人员提供一站式的RNA干扰相关服务。
总结
经过长期盛衰沉浮,反义技术近年来得到越来越多的注意。对能够提高靶表亲和性和生物稳定性、降低毒性的修饰核苷的研究取得了重要进展。由于大多数新的DNA类似物不能激活RNaseH,对反义寡核苷酸的设计需要考虑靶mRNA是否需要保留,例如,是改变剪接方式,还是降解靶mRNA(这种情况下应该使用gapmer技术)。可以通过有系统的修饰天然核酶或者通过体外选择技术获得具有高催化活性的稳定核酶。一些反义寡核苷酸和核酶已经进入临床试验研究,一个反义药物已经在1998年获得批准。一个重要的突破是发现短的双链RNA分子可用于哺乳动物细胞中特异性沉默基因表达。这个方法与传统的反义技术比效率明显更高,并且一些体内实验的数据已经发表。因此,反义技术有望广泛应用于对未知功能基因的研究、药物靶标的确认和治疗。









